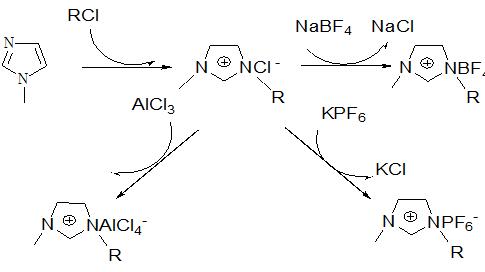
图1-1 合成离子液体的典型反应步骤
我们可以组合不同的阴阳离子合成所需的高极性化合物,因此根据合成的高极性化合物的需求为设计导向是实验中所要探讨的。
1.1.1.3高极性化合物的分类
高极性化合物一般来说有三种分类方法。第一类是Macfarlane等人提出的依照溶液的酸碱性将不同的离子液体分为酸性离子液体、中性离子液体和碱性离子液体。第二类是根据不同的阳离子作为标准,又将其分为4种:烷基季铵离子(NRxH4-x)+[12]、烷基季磷离子(PRxH4-x)+[13]、烷基取代吡啶离子(RPy)+[14]、烷基取代咪唑离子(PR’im)+[15]。除去以上四种常见离子液体,Shreeve等人还研究出了很多有特异性阳离子的离子液体。此外,以手性部队称结构、硫等结构的离子液体也不停的出现。
图1-2 几种常用的离子液体的阳离子
第三类是由不同阴离子将高极性化合物划分为两类:(1)AlX3与卤化盐(X可以是Cl或Br),如1-乙基-3-甲咪唑氯代铝酸盐([emim]Cl-AlCl3),不过此盐在水中很不稳定,需在空气或稳定的气氛中研究处理。另外,氧化物杂质可以很大程度上作用于有高极性化合物的反应过程。(2)AlX3与非卤化盐,此类新型离子液体的阳离子大多数是烷基取代的咪唑离子,阴离子为CH3COO-、CF3COO-、BF4-、PF6-等。这些离子液体能够较稳定的存在于水和空气中,如1-乙基-3-甲基咪唑四氟硼酸盐([emim]BF4)。
1.1.1.4高极性化合物的性质
(1) 溶解性
高极性化合物能够很大程度上使有机物溶解于此,这是因为高极性化合物的组成不仅有有机阳离子还有无机阴离子,所以高极性化合物拥有有机和无机物质的所有性能,或在两种物质之间的特性,是许多化学反应的良好溶解。将正辛烯溶解于甲苯磺酸盐阴离子季铵盐离子液体中,实验结果表明,当阳离子的侧链越长,正辛烯的溶解能力越好。与此同时,将水溶解于 [BMIM]+阳离子的高极性化合物中,水的溶解程度很大程度上取决于阳离子。许多高极性化合物的介电常数会超过一极限值,所以能和有机溶剂充分混合。
(2) 热稳定性
高极性化合物的热稳定性受限于碳原子和杂原子之间的作用力,以及氢键和杂原子之间的作用力,所以是与构成的阴阳离子的性质与结构紧密关联。高极性化合物在很大范围里都是很稳定的,许多季铵高极性化合物的极限温度在150 °C左右,[EMIM][(CE3SO3)]的热稳定性温度在400 °C以上。由此可知,与许多有机溶剂比较,高极性化合物有着更加宽的热稳定性温度。
(3) 粘度
高极性化合物的粘度取决于氢键与范德华力。由[BMIM]+组成的离子液体粘度比较低是因为其中侧链较短,比较活泼。然而含有较长烷基链的离子液体因为范德华力较大,所以有较大粘度。
由于范德华力所以含[C4F9SO3]-和[C3F7CO2]-的离子液体的粘度变大,所以从[CF3SO3]-到[C4F9SO3]-、[CF3CO2]-到[C3F7CO2]-,离子液体的粘度逐渐增加。 比较[BMIM][CF3SO3]和[BMIM][(CF3SO2)2N]的粘度可以发现,因为粘度增加是由于较弱的氢键抵消了范德华力,所以尽管含[(CF3SO2)2N]-的离子液体的范德华力很强,但粘度不大。
与此同时,因为咪唑阳离子中碱氯离子和氢原子之间形成氢键,当把含有不同组合的铝酸盐放在一起比较其粘度表明, 当物质三氯化铝变少,高极性化合物的粘度会逐渐变大。当高极性化合物呈现酸性的条件下,之所以粘度比较低是因为含有AlCl4-和Al2Cl7-阴离子很大程度上削弱了氢键。粘度数据表明,普通有机溶剂的粘度相较于离子液体的粘度要低1-2个数量级。 简单有机酸催化下的绿色高选择性氯代反应(3):http://www.youerw.com/huaxue/lunwen_12087.html

