3.3.6 温度对反应的影响 14
3.4 催化剂重复使用能力研究 14
3.5 底物拓展研究 15
3.6 锡改性皂土的催化机理 15
结 论 17
致 谢 19
参考文献 20
1 绪论
1.1 Baeyer-Villiger反应的相关背景
Adolf Baeyer以及Victor Villiger于1899年首次实现使用过硫酸将环酮氧化成相应内酯的反应,此后人们便将相关反应称作Baeyer-Villiger氧化反应[1]。其反应式可表示为:
对于Baeyer-Villiger反应,其具有以下优点:1.分子中其它官能团不受影响,例如不饱和酮在进行Baeyer-Villiger反应时与羰基不共轭的不饱和键不受影响。2.生成物的立体结构可以控制。3.可供选择的催化剂与氧化剂种类较多。这使得Baeyer-Villiger氧化反应在相关领域的应用越来越广。然而,在工业生产过程中,传统Baeyer-Villiger氧化反应仍存在许多不利因素,主要包括:1.氧化剂用量过大,使得在反应完成后残余大量废酸,对产物的分离造成一定困难且对环境不利;2.选择性差,当有与羰基共轭的不饱和键存在时,往往先氧化相应的不饱和键;3.当环酮具有旋光性时,往往得到消旋化产物。
Baeyer-Villiger反应的反应机理十分独特,其特殊的迁移机理以及很难被其它方法替代的特性,使得从1899年至今,众多学者仍在不断完善它的反应机理 [2 ,3]。最早,针对此反应Criegee提出了两步反应机理[4]:第一步是由过氧酸进攻羰基碳形成“Criegee”中间体,此中间体具有四面体结构。第二步为四面体中间体进行重排形成酯或内酯。按照Criegee中间体中O-O键断裂方式的不同,此过程又分为自由基型和离子型,O-O键均裂为自由基型,当其异裂时则属于离子型。
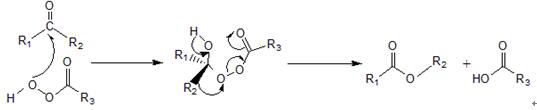
图1.1 Baeyer-Villiger氧化反应的两步机理。
1.2 Baeyer-Villiger氧化反应特点
针对Baeyer-Villiger氧化反应,主要有以下几方面特点:
1.反应中氧化剂强弱顺序为:三氟过氧乙酸>单过氧邻苯二甲酸>3,5-二硝基过氧苯甲酸>对硝基过氧苯甲酸>间氯过氧苯甲酸>过氧苯甲酸>过氧乙酸[5]。
2.不对称的酮在发生Baeyer-Villiger反应时常生成两种不同的酯,其取代基迁移的可能性称为迁移取向 [6]。不对称酮氧化时,与羰基相连基团的迁移倾向取决于其中心碳原子上电子云密度的大小,电子云密度大的亲核性强,其迁移倾向更大。
3.上面介绍到Baeyer-Villiger反应机理是生成“Cariegee”中间体的两步反应,因此存在反应过程中哪步是决速步的问题。二十世纪五十年代,Hawthorne和Emmons提出在Baeyer-Villiger反应中第二步(酸催化迁移)为决速步[7],Simamura等在进行反应动力学的研究后,也认为第二步的迁移是整个反应的决速步骤[8]。然而,随着人们的研究进展,发现参与反应的酮的自身性质(吸电子性还是给电子性)能够使决速步发生改变,也需要予以考虑。同时,研究发现一些催化剂对整体反应的决速步也有影响。在与不同催化剂所形成的催化体系中,反应的决速步会有所差别。因此可知,关于Baeyer-Villiger反应的机理,虽然人们进行了大量的研究,但相关机理的细节仍不明确,特别是对加入催化剂后的相关反应机理仍需深入研究。
1.3 Baeyer-Villiger反应的绿色氧化方法
在传统的工业生产中,往往采用过氧酸为氧化剂进行Baeyer-Villiger反应,虽然过氧酸氧化性强,但这类氧化剂并不是环境友好型的化学品,其在反应过程中产生大量副产物,处理不当便会对环境造成危害。随着近年来人们对绿色化学的关注度越来越高,人们迫切地想要寻找出一种新型氧化剂,在对环境影响较小的前提下取代目前广泛使用的过氧酸。从当下的研究进展来看,双氧水似乎是一种理想的替代品。与传统有机/无机过氧酸相比,其优势如下:双氧水为氧化剂可简化实验步骤,省略了有机过酸参与反应造成的副产品分离过程;在反应过程中无缓冲液的需求且产生的活性氧浓度较高,副产物仅有水,生成物洁净。因此,以双氧水为氧化剂应用于大规模的工业生产是一种十分理想的选择。但是,双氧水也有其自身的局限性:首先,与传统氧化剂过氧酸相比,双氧水氧化能力要弱得多;其次,在反应过程中双氧水不断分解,生成的水会使得到的产物发生水解,从而降低了反应的产率。 以双氧水为氧化剂的环酮的Baeyer-Villiger反应研究(2):http://www.youerw.com/huaxue/lunwen_14459.html

