1.1 锂离子电池的发展历史
1970年,埃克森(Exxon Corporation)的M.S.Whittingham采用硫化钛TiS作为正极材料,金属锂作为负极材料,制备出世界上首个锂电池。
1980年,J. Goodenough 发现钴酸锂LiCoO2可以作为锂离子电池正极材料。
1982年伊利诺伊理工大学的研究人员发现锂离子可以嵌入石墨,而且嵌入过程快速并且可逆,人们萌生了利用通过锂离子的脱嵌进行研究的想法。与此同时,采用金属锂制成的锂电池,存在着极大的安全隐患,因此人们尝试利用锂离子嵌入石墨的特性制作充电电池。同年,贝尔实验室成功试制了世界上首个可用的锂离子石墨电极。
1991年日本的索尼公司发布首个商用锂离子电池。该锂离子电池创新性地使用LiCO2作正极,炭材料为负极。电池的能量密度和循环性能相比于传统电池有了很大的提高。随后,众多的商业公司发现锂离子电池应用于电子产品的商业价值,锂离子电池的研究进入高潮期,开始了更加迅速的发展[2]。
随着时代的发展,越来越多的数码电子产品如手机、笔记本电脑等产品逐渐涌现,越来越多地成为人们生活的一部分,这些电子产品的电量存贮问题急需解决。锂离子电池以其优异的性能得到了广泛应用,目前市面上生产和应用最多的储能材料就是锂离子电池。同时,锂离子电池还在逐步向其他产品应用领域发展。习惯上,人们把锂离子电池也称为锂电池。但这锂电池和锂离子电池的工作原理和性能并不相同。我们现在研究、使用的一般均为锂离子电池,而发展更早的锂电池正逐渐被淘汰。
1.2 锂离子电池的工作原理
锂离子电池是指分别用二个能可逆地嵌入与脱嵌锂离子的化合物作为正负极构成的二次电池。
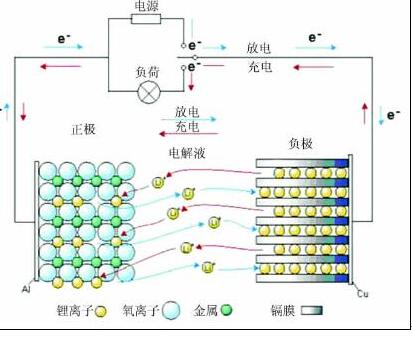
图1.1 锂离子电池的工作原理
锂离子电池的工作原理如图1.1所示。从原理上讲,锂离子电池实际上是一个锂离子浓差电池,正负电极由两种不同的锂离子嵌入化合物构成。充电的时候,Li+从正极脱嵌经过电解液嵌入负极,此时负极处于富锂态,正极处于贫锂态,也就是说负极的锂离子浓度高于正极;放电时则相反,Li+从负极脱嵌,经过电解质嵌入正极,正极处于富锂态,负极处于贫锂态,正极的锂离子浓度高于负极[6]。
锂离子电池的工作电压与两方面有关,一是构成电极的锂离子嵌入化合物本身,二是锂离子的浓度。因此,在充放电循环时,Li+分别在正负极上发生“嵌入-脱嵌”反应,Li+便在正负极之间来回移动,就好像摇椅一样。所以,人们又形象地把锂离子电池称为“摇椅电池”或“摇摆电池”[3]。
锂离子电池一般由正极、负极、电解液和隔膜四个部分构成。
锂离子电池的正极材料的要求是必须有能够接纳锂离子的位置和扩散路径,目前应用性能较好的正极材料是过渡金属氧化物和锂的化合物,其具有高插入电位的层状结构,如LixCoO2,LixNiO2以及尖晶石结构的LiMn2O4等[4]。负极材料一般用锂碳层间化合物以及各种碳素材料。 负极材料的研究相比于正极材料还很不成熟,目前阶段并没有比较完善的为所有人接受的材料,所以锂离子电池负极材料的研究具有很大前景和价值。
2 过渡金属磷化物作为锂离子电池负极材料的研究
2.1 负极材料的研究现状
2.1.1 负极材料发展历史
2.2 过渡金属磷化物为负极材料的研究现状
3 样品的制备及分析、测试方法
3.1 实验原料和仪器 Cu3P三维纳米线阵列作为锂离子电池负极材料的研究(2):http://www.youerw.com/huaxue/lunwen_19270.html

