这些年随着炼铁炼钢、电镀等工业的发展,水体中Mn2+、Cr3+、Pb2+、Hg2+等金属离子的浓度增加很多,这种有毒的重金属元素的溶解和释放影响到了水中的生态平衡,并且会通过渗透作用污染地下水[2],这危害到了人类的健康。此外,大量金属离子会通过原电池作用引起水电设备的锈蚀;灌溉作用也会使水体中的重金属离子进入土壤,导致土壤污染,会对农业生产产生不良影响[3]。因此,我们要对水体中的离子种类进行识别,并对其浓度进行检测。但是,现在可以用于阳离子识别的体系较少,因为受体对金属阳离子的结合和识别能力受到多种因素的影响,其中最主要的难点是受体有可能与体系中的其他金属阳离子相结合,这样就难以只对一种离子进行单一性的信息响应。
现在,科研人员在电化学传感技术和荧光传感技术的基础上合成了比较多的受体分子,其中某些受体分子能在其他阳离子的存在的条件下单一性的识别一种离子,而且其信号强烈,容易辨识,简化了检测的步骤,缩短了检测的时间。
1.1 二茂铁及其衍生物概论
1.1.1 二茂铁的发现
二茂铁是不经意间被发现的,事情发生在1951年,杜肯大学的Kealy和Pauson正在用环戊二烯基溴化镁处理氯化铁,尝试去得到富瓦烯,但是失败了,不过却很偶然地得到了一种橙黄色固体[4],它的性质很稳定。于是他们对它进行了简单的研究,最后得出这个物质的分子式是 C10H10Fe,而且还得出此物质的一些物性,比如该物质不溶于水,但易溶于乙醇、二氯甲烷、石油醚和甲醇等常用有机溶剂,它的熔点是172.5~173℃,沸点为 249℃,整体比较稳定。不过当时的研究条件有限,他们并没有确定这种物质的结构,也没有继续研究该物质的更多性质。所以当时他们猜测二茂铁的结构不是夹心的,并认为它的稳定性是由于它的芳香的环戊二烯基负离子。在同一时间,Tremaine、Miller和Tebboth以一种还原铁为催化剂,在常压300℃的条件下,将环戊二烯与氮气混合后,也得到了这种橙黄色固体,即二茂铁。
1.1.2 二茂铁的结构的研究
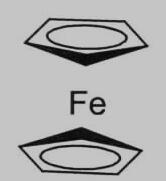
虽然Kealy等人发现了二茂铁,但他们未能确定它的结构,不过他们还是将他们的发现以及研究结果发表在1951年的Nature杂志上,1952年,Tremaine 等人也在J.Chem.Soc.杂志上发表了他们的发现,这几篇文章引起了许多科学家的兴趣。Fischer等人使用X射线衍射的研究,提出这种物质拥有五角反棱柱的结构。Wilkinson等人通过偶极距、磁化率及红外光谱等的测定,判断出此物质拥有夹心型的结构。正是通过这些研究,最终我们确定了该物质的结构,它上下各有一个相同的带负电的环戊二烯基芳环,中间是一个带有正二价正电荷的铁离子,形状如同三明治(如图1.1),所以也有人称它为“三明治化合物”,最后,二茂铁成为了它的正式名。这些研究促进了人们对二茂铁及其衍生物更多的研究,也推动了金属有机化学的发展,所以,Fischer和Wilkinson两人一起获得了1973年的诺贝尔化学奖。
图1.1 二茂铁的夹心结构
1.1.3 二茂铁及其衍生物的应用
二茂铁具有易取代、稳定性、亲油性、芳香性、低毒、氧化还原性和富电性等许多特点,所以自从二茂铁出现以后广大科研人员就一直关注与研究着它。100多年来,人们从未停止过对二茂铁及其衍生物的结构、性质、设计、合成和应用的研究。现在,有了科技的发展,还有着广大科研人员的努力,二茂铁及其衍生物在分析化学、催化、功能材料和生物医药等多个领域有了非常多的应用。 N-吡啶二茂铁基阳离子探针分子的合成及应用(2):http://www.youerw.com/huaxue/lunwen_35413.html

