在这种情况下,鉴于环戊烯酮衍生物的应用潜力之大,大量的注意力被投入到取代环戊烯酮的合成制备及其动力学拆分上。近年来,4-羟基-2-取代基-2-环戊烯酮这类化合物的几个代表已经成功制备,并且通过使用不同的脂肪酶和酰化试剂它们也得以拆分。许多文献中也发展了不少关于制备4-羟基-2-取代基-2-环戊烯酮这一类光学纯化合物的合成方法,包括烯丙醇底物的去对称化以及酶催化的动力学拆分反应,均取得了优异的对映选择性。然而,对于4-羟基-5-取代基-2-环戊烯酮的不对称合成方法,几乎没有与之密切相关的报道。主要原因是这类化合物在C-5位置上存在差向异构作用,比较容易消旋化,而且该化合物本身也不够稳定,在一定的酸碱条件下易发生逆羟醛缩合反应(Retro-Aldol Reaction),使得不对称合成成为难点。直到最近才由波兰的Wicha小组报导了首例的不对称合成工作[11]。但是该类化合物的底物范围和应用价值仍没有进行深入的研究与探讨,而且脂肪酶CAL-B的催化效率依然不够理想。
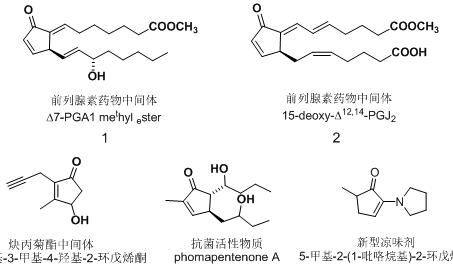
图1 各类环戊烯酮衍生物
然而,经典动力学拆分法自身所存在的缺陷难以克服,光学纯手性化合物的最大理论产率仅仅只有50%,另一半只得废弃且难以继续回收利用。这不仅会对环境造成不必要的污染,而且也违背了原子经济原则[8]。而动态动力学拆分(Dynamic Kinetic Resolution,DKR)的兴起彻底击溃了经典动力学拆分法原有的缺陷之墙。它是经典动力学拆分与底物消旋化的结合体。即在动力学拆分进行的同时,加人手性试剂使底物完全消旋化并将预舍弃的对映体立体转化,进而分离以得到某一光学纯对映体。在此历程中,底物常常会被转化成非对应异构体产物,或者是将外消旋混合物全部转化成所需要的纯手性化合物,理论产率为100%。目前,光学纯手性化合物的获得途径主要有不对称合成法、化学法、生物酶催化法以及色谱法等等[9-10]。其中生物酶催化拆分法,与其他方法相比,因具有更高效、更环保、反应条件更温和等优势而深受人们的青睐。作为一种绿色高效的催化剂,生物酶不仅在某些合成工艺中成为了传统金属催化和化学催化的有益补充,而且也极大地拓宽了其作为催化剂的应用范围。随着现代科学技术的不断发展与突破,特别是仪器分析技术的崛起,色谱技术已然成为当前手性分离的主要科学工具。其中,高效液相色谱对于对映体分离的研究较为成熟,其分析范围广,灵敏度高,操作灵活简单,选择性高,对手性物质的分析及分离方面具有决定性的优势,因此也一直成为人们分离测定手性化合物拆分效果的重要分析工具。
1.2 动力学拆分简介
动力学拆分是实现对映异构体拆分的一种较为常见的方法,它是指在对映异构体体系中加入手性试剂,与之反应生成非对映异构体。由于原先的一对对映异构体在生成非对映异构体时的反应活化能存在明显差异,故手性试剂进攻两个对映体的速率也大不相同。对映体相互竞争,在一定时间内,反应速率快的将优先与手性试剂完成反应,反应速率慢的则会被剩下,从而进一步实现光学纯化合物的获取。
早在1858年,Pasteur[11]便成功开启了化学史上第一个运用动力学拆分的例子。他发现用灰绿青毒霉发酵消旋酒石酸钱时, 左、右旋对映异构体的代谢速度不一,并以此进行分离得到了光学活性化合物。直到1981年,sharples[12]等人报道了在不对称环氧化反应的条件下外消旋烯丙仲醇的底物回收对映体过量达到了90%以上。动力学拆分在手性合成中才变得实用起来。原经典动力学拆分的最大理论产率为50%,之后兴起的动态动力学拆分不仅完美跨越了这道坎,而且人们还将其与底物的现场立体转化结合, 大大提升了单一对映体的产率, 并且实现了在理想状态下得到对映体过量均为100%的单一光学纯产物。1997年vedej和ehen又提出了一种新的平行动力学拆分法, 再次丰富和发展了这一研究领域。而今,手性拆分的热门方法无疑是动态动力学拆分,在进行动力学拆分的同时加入消旋催化剂将无用的光学异构体现场立体转化, 从而达到由消旋体直接转化成单一光学纯度化合物的方法,该法克服了经典动力学拆分最高产率只有50%的缺陷,在反应效率和应用范围方面均取得了巨大的进步,是目前手性拆分方法研究的一个新的热点。 取代环戊烯酮的酶催化动力学拆分(3):http://www.youerw.com/huaxue/lunwen_29918.html

