m) 绿色环保性能高:锂离子电池的负极材料一般采用可以自由脱嵌锂离子的材料,一般情况下对环境影响较小,而其正极材料通常情况下是Li的过渡金属氧化物,对环境危害很小,并且不含有汞、银、镉等重金属物质,同时电池被很好地密封,整个电池形成一个封闭的体系,不会对环境造成污染。
n) 自放电率小且无记忆效应:锂离子电池的月平均自放电率一般在6-8%左右,而镍镉和镍氢电池为前者的两倍以上。传统的铅酸(或胶体)电池在充放电循环过程中,电池的容量会随着使用时间的增长而变小,这种现象叫做记忆效应,是传统电池行业中很重要的一个问题。但是锂离子电池不存在这种效应。
1.1.1 锂离子电池的工作原理
锂离子电池是一种新兴的将化学能与电能相互转化的装置,其主要的结构可大致分为三类:电极材料(包括电池正、负极材料)、电解液和隔膜。电池的正负极材料直接影响着电池的性能好坏,正极材料通常由能够自由脱嵌Li+的化合物构成。电解液的主要作用是传输和承载Li+,并且锂离子电池的导电性也是由电解液来实现的,所以锂离子电池中的锂离子主要集中在电解液中。隔膜是位于正负极材料之间的一种离子半透膜,其主要的作用是防止电池正负极相接触发生短路,还能够顺利的让离子通过,从而实现电池中的电化学反应。
当电池充电时,正极中的Li+从材料中脱嵌出来,先进入电解液中,再通过隔膜嵌入负极材料中,此时的正极材料处于贫锂状态;与此相反,电池放电的时候,Li+从负极材料中脱出,同样先进入电解液中,再通过隔膜嵌入到正极材料中,此时的正极材料为富锂状态。根据电荷守恒定律,充放电过程电子经过外界电路转移的电子的数量是相等的,可以理解为Li+在充放电过程中在正、负极之间不断移动,正极与负极之间发生了氧化还原反应,从而可以保持电位稳定。Li+的脱出和嵌入,可能会使正负极材料之间的层间距发生变化,不过对材料的晶体结构没有显著的影响,基于以上的特性,锂离子电池的安全性以及稳定性才有保障。锂离子电池的工作电位由锂离子电池正、负极材料中能够自由脱嵌Li+的化合物的化学性质以及Li+的浓度等决定[8]。
锂离子电池的反应本质上与锂离子浓差电池的反应原理基本相同。
从图1能够直观地看出,锂离子电池实质上是一个锂离子浓差电池,两种不同的锂离子嵌入化合物形成了锂离子电池的正极和负极。
锂离子电池正负极反应化学方程式为:
正极反应: 1.1
负极反应: 1.2
电池总反应方程式:
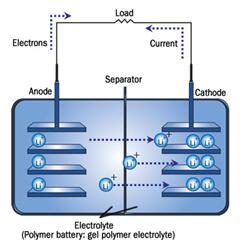
图 1 锂电池工作原理
常用的正极材料有:LiCoO2、LiMn2O4、Li3V2(PO4)3、LiFePO4等,常用的负极材料有:LixC6、Li4Ti5O12等。
1.1.2 锂离子电池正极材料
就目前锂离子电池的发展情况来说,主要的研究方向应该朝着制备出更高容量的正极材料方面前进,事实上可以自由嵌入脱出Li+的物质非常多,可真正能够满足锂离子电池正极材料性能需求的材料为数不多。 微波溶剂热法制备锰取代磷酸钴锂正极材料及其电化学性能表征(3):http://www.youerw.com/huaxue/lunwen_25513.html

