多糖合成途径中功能基因的鉴定及其在粘细菌发育中的研究(3)
时间:2018-07-10 10:37 来源:毕业论文 作者:毕业论文 点击:次
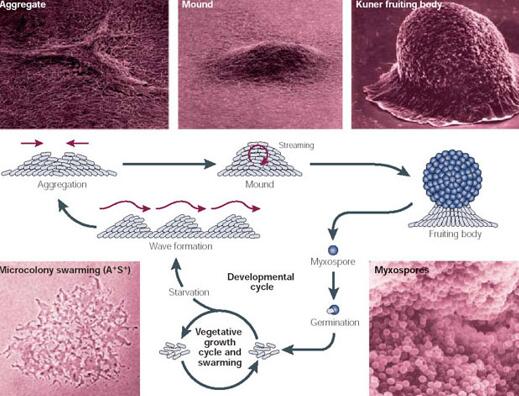 图1-1-1 粘细菌多细胞发育进程[5] Fig. 1-1-1 Coupling movement to multicellular development in myxobacteria[5] 粘细菌的滑行运动受两个清楚的遗传系统调控,一个是细胞的单独运动——A运动 (adventurous motility) ,另一个是细胞群体的运动——S运动 (social motility)[9]。S运动对于黄色粘球菌生命周期的各个阶段的行为是非常重要的[6, 7],与粘细菌的发育、运动和捕食等行为息息相关。粘细菌的S运动系统至少需要细胞表面三种组成部分:脂多糖 (lipopolysaccharide,LPS) -O-抗原、四型菌毛 (type IV pili,TFP) 和胞外多糖 (exopolysaccharides,EPS) 。 胞外多糖在不同来源的菌株中发挥中重要的作用。在共生固氮菌R.meliloti中,EPS对于在植物寄主上形成根瘤发挥关键作用[10, 11],E. coli中EPS是感染寄主的关键因子[12]。粘细菌的胞外基质中由蛋白和EPS组成,蛋白与EPS的比例约为1:1.2。目前从黄色粘球菌中分离出八种单糖,包括葡萄糖、鼠李糖、甘露糖、N-乙酰葡糖胺、N-乙酰甘露糖胺、半乳糖、木糖和阿拉伯糖[2]。有趣的是,尽管黄色粘球菌产生一定数量的聚糖,但是这种需氧的微生物却不利用环境中的单糖作为碳源和能源[13-16]。考虑到它不利用葡萄糖,那么在糖异生途径中就一定存在某些关键的酶催化合成EPS中的各种单糖组分。每一种磷酸化单糖的产生涉及到多个功能蛋白,包括糖基转移酶,异构酶以及脱氢还原酶等,构成了特殊的糖代谢途径。目前已经鉴定出多个参与单糖代谢的功能基因。 众多研究表明粘细菌的胞外基质多糖对粘细菌的运动性、子实体结构的形成以及细胞间的信号传递有着重要作用。尽管已经有很多研究阐明了EPS的合成机制,但大部分的研究都集中在糖聚合和转运的过程,针对EPS的磷酸化单糖组分合成途径中的部分关键酶的具体功能尚不明确。因此,本研究通过文献调研和前期工作的基础上拟筛选出五个参与粘细菌单糖合成的关键基因,利用基因插入失活的分子生物学技术,验证这几个关键酶对EPS合成的作用,同时对EPS在粘细菌发育过程中机制进行初步的研究。 1 材料方法 1.1 菌株和质粒 表2-1-1 供试菌株与质粒 Table 2-1-1 Strains and plasmids used in this study 菌株和质粒 特征 来源 Strains M. xanthus DK1622 Wild type Kaiser D. and Mao xiaohua CL2001 DK1622,MXAN_2921::kan This study CL 2002 DK1622,MXAN_3506::kan This study CL 2003 DK1622,MXAN_4613::kan This study CL 2004 DK1622,MXAN_5333::kan This study CL 2005 DK1622,MXAN_6908::kan This study E. coli DH5α Host strain for cloning vectors TransGen Biotech β 2155 Diaminopimelic acid (DAP) auxotroph Bei weicheng Plasmids pMD19-T T-A clone vectors, Ampr TaKaRa pMD19-T- 2921 pMD19-T derivative carrying MXAN_2921 This study pMD19-T- 3506 pMD19-T derivative carrying MXAN_3506 This study pMD19-T- 4613 pMD19-T derivative carrying MXAN_4613 This study (责任编辑:qin) |